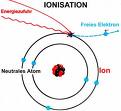
Ionisation
L'ionisation est l'action qui consiste à enlever ou ajouter des charges à un atome ou une molécule. L'atome - ou la molécule - en perdant ou en gagnant des charges n'est plus neutre électriquement.

Catégories :
Physique atomique - Physique quantique - Thermodynamique - Électrochimie - Chimie quantique
Recherche sur Google Images :
Source image : forums.futura-sciences.com Cette image est un résultat de recherche de Google Image. Elle est peut-être réduite par rapport à l'originale et/ou protégée par des droits d'auteur. |
Définitions :
- Processus durant lequel un atome ou une molécule perd ou gagne des électrons, acquérant une charge électrique ou modifiant une charge existante (source : mmfai)
L'ionisation est l'action qui consiste à enlever ou ajouter des charges à un atome ou une molécule. L'atome - ou la molécule - en perdant ou en gagnant des charges n'est plus neutre électriquement. Il est alors nommé ion.
Les applications sont nombreuses :
- décontamination alimentaire
- modifications des plastiques
- stérilisation des matériels médicaux
- étude des matériaux
- etc.
Énergie de première ionisation
C'est l'énergie indispensable pour extraire le premier électron (c'est-à-dire l'électron dont l'énergie de liaison est la plus faible) de la structure atomique.
Formule générique décrivant l'ionisation à un électron : X → X + + e −
Impact électronique
Ce type d'ionisation est fréquemment utilisé en spectrométrie de masse. Un électron émis par un filament rencontre l'atome ou la molécule et lui arrache lors du choc un de ses électrons (spectrométrie de masse).
Exemple avec le méthane : CH4 + e − → 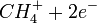
Photo-ionisation
L'ionisation peut être réalisée par des rayonnements de longueur d'onde suffisante pour éjecter cet électron périphérique. Quand le rayonnement ionisant est constitué de photons, on parle de photoionisation. C'est par exemple ce qui se passe dans les nébuleuses planétaires.
Ionisation thermique
Si on apporte suffisamment d'énergie thermique à un gaz, son énergie moyenne peut devenir identique ou supérieure à son énergie d'ionisation. Les constituants de ce gaz peuvent par conséquent s'ioniser sous les chocs entre atome/molécule. C'est ce qui arrive dans la couronne solaire.
L'énergie moyenne d'un gaz parfait est identique à 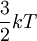 , ou plus exactement à
, ou plus exactement à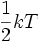 par degré de liberté.
par degré de liberté.
k correspond à la constante de Boltzmann.
T correspond à la température.
Ionisation chimique
C'est une réaction entre une molécule et un ion réactant. Le résultat donnera lieu a un transfert d'électrons ou à la création d'adduit.
Exemple avec une molécule M :
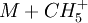 → MH + + CH4
→ MH + + CH4
- Film pédagogique ancien, Ionisation des gaz de Maurice Françon, couleur
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 13/04/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.

 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité