Liaison π
La liaison π est une liaison chimique covalente qui est créée entre deux atomes par recouvrement d'orbitales de nombre quantique secondaire > 1.
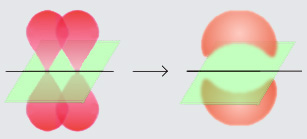
La liaison π est une liaison chimique covalente qui est créée entre deux atomes par recouvrement d'orbitales de nombre quantique secondaire > 1 (orbitales p, d…). Le recouvrement est latéral, c'est-à-dire que les 2 lobes des deux orbitales en interaction sont parallèles, contrairement au cas des liaisons σ où les lobes des 2 orbitales atomiques pointent l'un vers l'autre.
La liaison π est présente surtout dans les alcènes et dans les alcynes :
- alcènes : présence de liaisons doubles dans un squelette carboné ;
- alcynes : présence de liaisons triples dans un squelette carboné.
La présence d'une liaison π empêche toute libre rotation autour de cette liaison, car elle entraîne une rigidité moléculaire. C'est à cette rigidité qu'est due la stéréoisomérie de certains alcènes ou alcynes. De plus, la liaison π permet les réactions d'addition, car elle se casse aisément, à l'inverse de la liaison σ. A titre d'exemple, l'ajout de diiode sur le propyne se fait par rupture des liaisons π (il reste toujours la liaison σ).
Une molécule qui possède plusieurs liaisons π (ou une liaison π et des doublets non liants ou des lacunes électroniques) présente la caractéristique de posséder plusieurs formes mésomères : les électrons sont délocalisés.
Une liaison π est moins forte qu'une liaison σ, en moyenne, une liaison π entre deux atomes de carbon a une énergie de 250 kJ. mol-1.
Recherche sur Google Images : |
|
"Cyb@rdèche: un accompagnement sur ..." L'image ci-contre est extraite du site www.cybardeche.fr Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (1606 x 2319 - 1016 ko - jpg)Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 13/04/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité